
近日,同济大学附属同济医院普通外科胡志前主任、李新星副主任医师团队联合同济大学生命科学与技术学院徐艳萍教授团队,在国际顶级学术期刊Molecular Cancer(影响因子约34)发表了重磅研究成果。论文题为Immune-related deubiquitylation spectrum of microsatellite stability colorectal cancer reveals USP7 as a potential immunotherapeutic target(微卫星稳定型结直肠癌的免疫相关去泛素化谱揭示 USP7为潜在免疫治疗靶点)。该研究由同济医院印小毛博士担任第一作者,胡志前和李新星共同担任通讯作者。该成果代表了同济医院在肿瘤免疫微环境与去泛素化调控研究领域的最新突破,更彰显了医院在临床与基础转化研究融合进程中的关键跨越。
该研究聚焦于当前国际结直肠癌研究中的重大难题——微卫星稳定型(MSS)结直肠癌的免疫冷表型形成机制。据悉,MSS型肿瘤约占结直肠癌患者的90%以上,但其对免疫检查点抑制剂(ICIs)几乎无应答,长期以来是免疫治疗的“瓶颈”,亟待机制突破与靶向策略革新。
研究团队基于临床样本和多组学技术(涵盖转录组、蛋白质组和免疫组化分析),系统解析了MSS型结直肠癌的免疫去泛素化谱,首次揭示去泛素化酶USP7在肿瘤免疫逃逸中的核心调控作用。研究发现,USP7通过稳定关键抑制蛋白并下调CXCL9/10–IFNγ信号通路,抑制 CD8⁺ T细胞的浸润与活化,从而导致肿瘤免疫冷环境形成。相反,当通过药物或基因手段抑制USP7活性后,肿瘤微环境中的免疫细胞显著活化,细胞毒性增强,提示USP7可能成为MSS型结直肠癌免疫治疗的全新分子靶点。
该研究建立了MSS型结直肠癌“去泛素化–免疫抑制”新机制模型,揭示了免疫逃逸的关键分子环节,为后续临床开发USP7靶向抑制剂联合放化疗或免疫疗法提供了坚实的理论依据。论文的成功发表,是同济医院长期坚守“临床需求牵引、基础研究赋能”协同创新理念的重要成果,充分展现了团队在多组学分析、肿瘤免疫机制解析以及转化医学研究领域的系统攻坚实力。
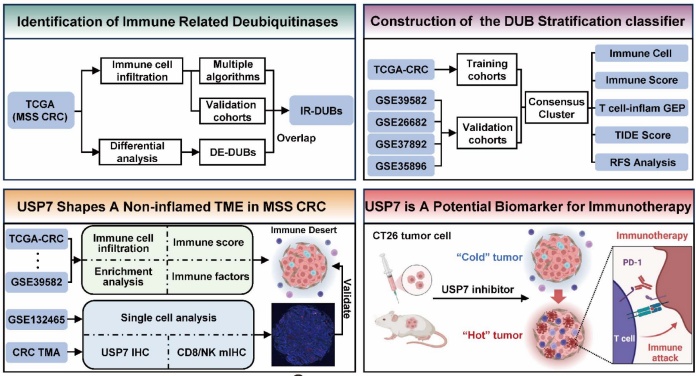
胡志前强调,本研究的成果不仅在机制层面拓展了对MSS型结直肠癌免疫耐受的认识,更为临床精准治疗提供了可转化的思路与药物靶点;李新星表示,团队未来将继续深入探讨去泛素化调控与代谢、免疫互作网络的交叉关系,推动MSS型结直肠癌免疫治疗策略的临床应用;徐艳萍指出,该研究充分彰显了医学院与生命科学学院的跨学科融合科研优势,为基础研究成果快速转化为临床诊疗手段提供了可复制的成功范例。。
此次论文的发表,标志着同济医院在结直肠癌免疫微环境研究领域取得了国际化原创成果,进一步提升了医院在肿瘤精准治疗与分子靶向研究方面的学术影响力。
图文|普通外科
编辑|张鹰妮
责任编辑|谢壮丽
