编译:高杰
皮肤发炎痊愈后,
为什么总在同一部位反复发作?
《Science》发表的一项最新研究
给出答案——
皮肤干细胞拥有炎症“记忆”,
而这种记忆能持续多久,
由DNA序列本身决定。
传统观点认为,炎症记忆是免疫细胞的专属功能。而洛克菲勒大学Elaine Fuchs 团队早在2017年就发现,表皮干细胞可储存长期炎症表观遗传记忆。
这项最新研究中,研究团队以小鼠表皮干细胞为模型,追踪长达约2年(接近小鼠整个生命周期)发现:绝大多数炎症相关染色质开放状态会逐渐消退,但约10-15%的记忆结构域能持久保持开放,炎症消退后仍保持“待命状态”,一旦再次受到刺激,就会快速启动强烈反应,这也是银屑病、湿疹等疾病反复复发的重要原因。
研究指出,组织会长期储存炎症“记忆”,提升对后续刺激的敏感性,但这些记忆如何跨越细胞分裂长期维持,一直是未解之谜。

研究团队面临一个难题:短效记忆与长效记忆的DNA序列看起来极为相似,该如何区分?
为此,他们开发了名为PersistNet的深度学习模型,专门用于捕捉记忆随时间的持续存在能力。模型迅速识别出关键特征:CpG二核苷酸密度。
CpG密度就像内置在DNA里的定时器:CpG含量越高,炎症记忆越持久。在近1000个记忆区域中,只有CpG密度能准确预测每个记忆的持续时间,其他序列模式均无法做到。
短期记忆区域CpG密度低,染色质状态会逐渐关闭;高CpG区域则能长期保持开放,让炎症记忆稳定跨细胞代际传递。
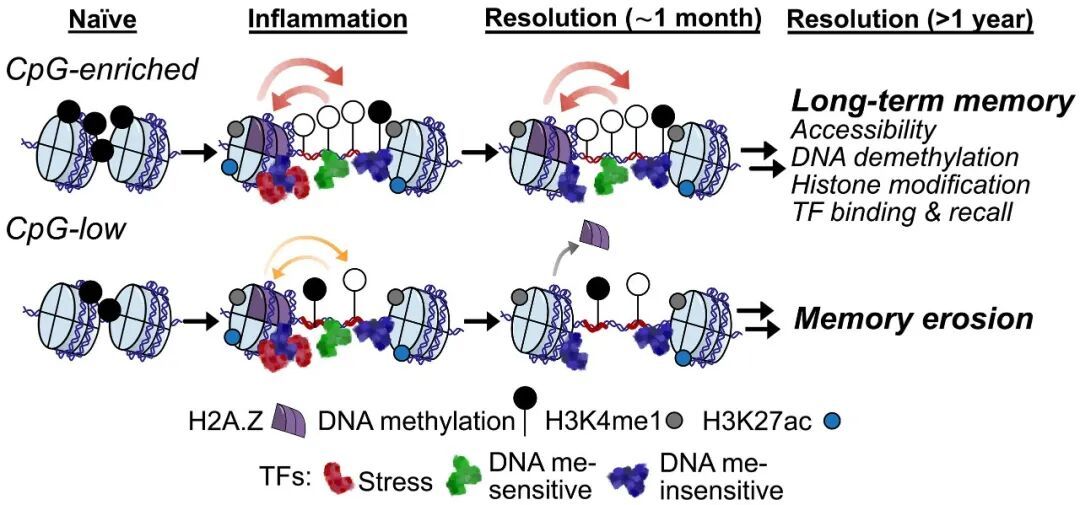
CpG序列本身并不参与记忆的建立,记忆启动仍依赖炎症诱导的转录因子打开染色质。但一旦记忆建立,这些CpG序列就变得至关重要,并通过4大机制稳定染色质开放。
具体来说,高CpG序列会在炎症后促使相关位点发生DNA去甲基化,并结合对甲基化状态敏感的转录因子来维持染色质开放;这类序列天生就不利于核小体组装,能减少染色质折叠,同时它还引入稳定性较弱的组蛋白变体H2A.Z,进一步削弱核小体紧密程度并抑制DNA重新甲基化,最终实现染色质开放状态的长期维持。
这4种机制协同作用,让高CpG区域的染色质像一扇“开放的大门”,即使经过多次细胞分裂,仍能保存炎症记忆。
“在前端,你仍然需要急性炎症体验来打开染色质。然后,根据调入了多少CpG,你要么拥有短期记忆,要么拥有长期记忆。”论文共同第一作者Christopher J. Cowley表示。
这项研究解决了一个长期存在的悖论:理论上,表观遗传标记会随细胞分裂不断稀释,但临床上,银屑病等疾病的炎症记忆却能长期存在。
该研究完美弥合了这一矛盾:高CpG序列通过自我强化的表观机制,主动维持染色质开放,而非被动保留标记,因此记忆不会随细胞分裂消失,而是稳定传递。
研究进一步在胰腺细胞、造血干细胞中验证,CpG密度调控炎症记忆寿命的机制在多种组织中普遍存在,具有高度保守性。
“我们的研究弥合了记忆持续性的机制理解与在临床环境中观察到的生理表现之间的差距。”论文共同第一作者Sairaj M. Sajjath表示。
这一发现为慢性炎症性疾病的治疗开辟了全新路径。传统治疗仅缓解急性症状,无法清除持久表观印记,这是疾病易复发的关键。未来,靶向高CpG序列的DNA甲基化状态、H2A.Z沉积等表观遗传调控点,有望精准“删除”病理性炎症记忆,从根源上治愈慢性炎症。
Elaine Fuchs教授指出,这些发现不仅为开发慢性炎症的新治疗策略提供切入点,也可能延伸至癌症、疼痛和体重反弹等其他疾病,因为这些疾病都与身体细胞的“异常记忆”密切相关。研究团队下一步将更多关注可能导致慢性炎症性疾病和癌症风险升高的不适应记忆,精准识别“坏记忆”的独特特征,以打破炎症疾病反复发作的恶性循环。

数据图及参考来源:
https://www.science.org/doi/10.1126/science.adz6830
除已标注来源外,本文封面图及文内图片均来自包图网(获授权使用),转载可能引起版权纠纷。